近日,医学院王祥虎团队联合美国明尼苏达大学The Hormel Institute在国际肝病学领域权威期刊Hepatology(中科院1区Top期刊,IF:12.6)和美国胃肠病学会(American Gastroenterology Association, AGA)官方基础研究期刊Cellular and Molecular Gastroenterology and Hepatology(CMGH)(中科院1区,IF:7.1)连发两篇重要研究论文。这两项研究聚焦于肝星状细胞(HSCs)在结直肠癌肝转移中的能量代谢调控机制,为相关疾病的治疗提供了全新视角和潜在靶点。
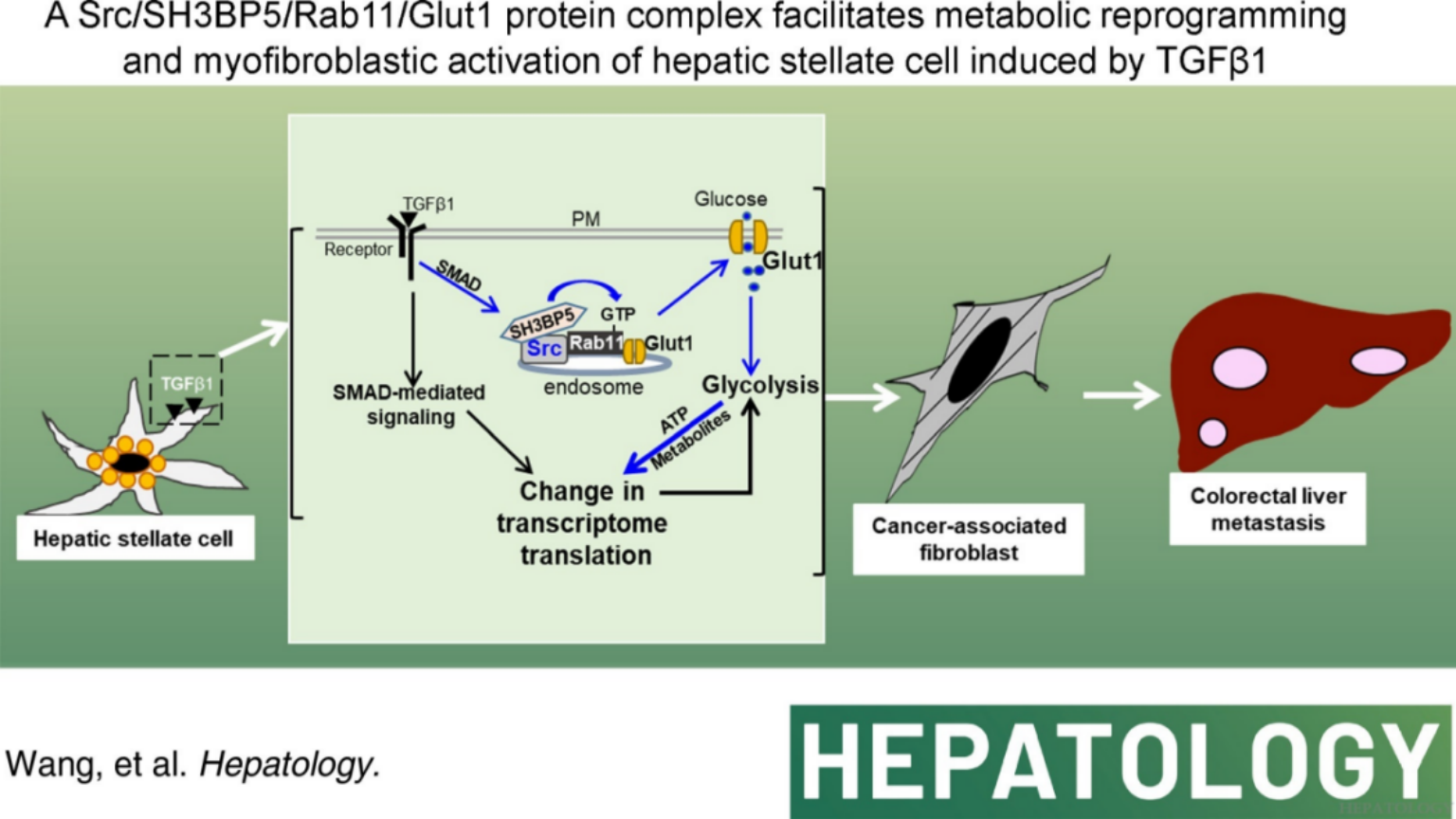
在Hepatology发表的研究论文《Targeting Src SH3 Domain–Mediated Glycolysis of HSC Suppresses Transcriptome, Myofibroblastic Activation, and Colorectal Liver Metastasis》中,研究团队探讨了葡萄糖转运蛋白1(Glut1)介导的糖酵解过程在HSCs向癌相关成纤维细胞(CAFs)转化中的核心作用。通过使用Cre/LoxP系统特异性敲除小鼠HSCs中Glut1,以及结合生物素标记和Seahorse XFe96分析技术,研究深入解析了Glut1在HSCs细胞膜上的分布及其代谢调控机制。团队发现,Src SH3结构域通过与SH3BP5蛋白结合,形成Src/SH3BP5/Rab11/Glut1复合体,在TGFβ1刺激下,激活了Rab11依赖的Glut1细胞膜转运,进而显著增强HSCs的糖酵解过程。小鼠模型实验证实,靶向Src SH3结构域能够有效抑制CAFs活化及结直肠癌肝转移,为靶向治疗提供了新思路。
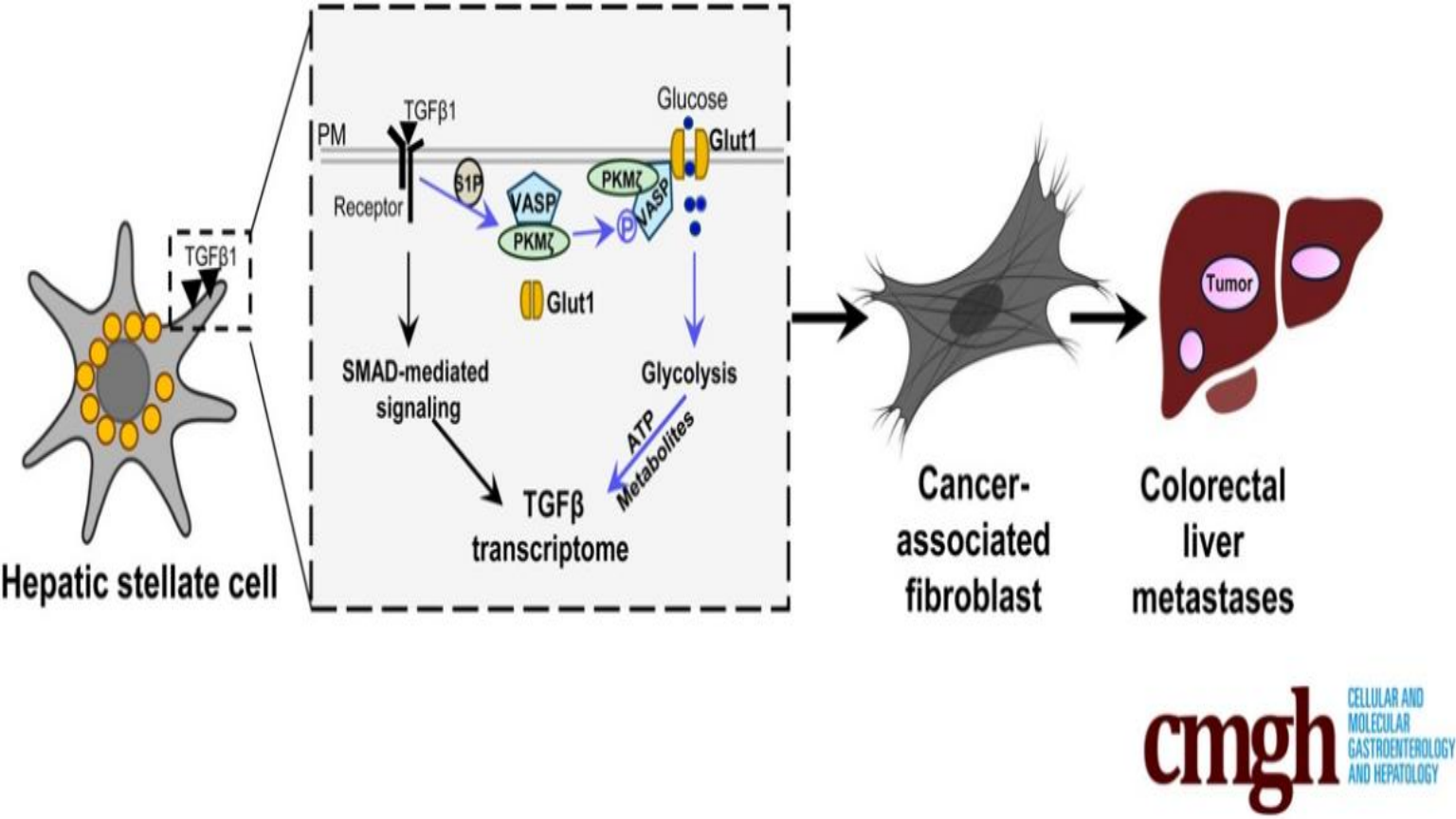
在另一篇发表于CMGH的论文《PKMζ, a brain-specific PKCζ isoform, is required for glycolysis and myofibroblastic activation of hepatic stellate cells》中,研究进一步揭示了蛋白激酶Mζ (PKMζ) 在HSCs代谢重编程与激活中的关键作用。研究表明,PKMζ通过促进血管舒张刺激磷酸化蛋白(VASP)在特定位点的磷酸化,帮助Glut1精准定位至细胞膜,驱动HSCs的糖酵解和激活。更重要的是,PKMζ在结直肠癌肝转移微环境中的CAFs中显著高表达,而靶向PKMζ可抑制HSC的CAF样激活,阻止肝转移肿瘤的生长,并改善肝纤维化。这一研究不仅揭示了TGFβ1调控HSC代谢和活化的新机制,还为肝纤维化及结直肠癌肝转移相关疾病的治疗提供了重要理论基础和临床潜力。这两项成果标志着王祥虎博士团队在肝纤维化和肿瘤微环境领域的研究迈上新台阶,为相关疾病的机制研究和精准治疗提供了新的研究方向,具有重要的科学价值和临床意义。
以上两项研究均由台州学院医学院与美国明尼苏达大学The Hormel Institute Prof. Ningling Kang团队合作完成,台州学院为主要合作单位。王祥虎博士分别为两篇论文的共同第一和第一作者。此外,特别感谢台州学院贺连平博士和安徽理工大学公共卫生学院王甜博士作为参与作者,为研究顺利完成提供了重要支持。
文章1链接:https://pmc.ncbi.nlm.nih.gov/articles/PMC11266532/
文章2链接:https://www.cmghjournal.org/article/S2352-345X(24)00184-X/fulltext
文:王祥虎/图:王祥虎/审核:林海斌、胡琼莹/责任编辑:徐贤